| 王慧娟,郑州大学附属肿瘤医院/河南省肿瘤医院内科副主任医师,副教授,硕士研究生导师。主要从事肺癌的临床与基础研究,具有丰富的临床实践经验,擅长肺癌的靶向、免疫及个体化综合治疗。目前担任中国临床肿瘤学会(CSCO)青年委员会常务委员,CSCO免疫治疗专家委员会委员,国际肺癌研究会(IASLC)会员,中国抗癌协会肺癌专业委员会青年委员会委员,河南省抗癌协会肺癌专业委员会青年委员会主任委员,河南省抗癌协会神经内分泌肿瘤专业委员会副主任委员,河南省老年学会肿瘤专业委员会常务委员,河南省抗癌协会化疗专业委员会、肿瘤标志专业委员会、肺癌专业委员会常务委员。发表专业论文40余篇,SCI论文8篇,获河南省科技进步二等奖3项,河南省医学科技进步二等奖1项,河南省医学新技术引进奖1项。 |
Peters S, Camidge DR, Shaw AT, et al. Alectinib versus Crizotinib in untreated ALK-positive non-small-cell lung cancer[J]. N Eng J Med, 2017, 377(9):829-838.
1b。
阿来替尼是间变性淋巴瘤激酶(anaplastic lymphoma kinase, ALK)的高选择性抑制剂。
与克唑替尼不同, 阿来替尼更容易穿透血脑屏障。在临床前和前期临床研究中, 阿来替尼在全身和中枢神经系统(central nervous system, CNS)都是有效的。
比较阿来替尼与克唑替尼在未经治疗的晚期ALK阳性非小细胞肺癌(non-small cell lung cancer, NSCLC)患者(包括无症状的CNS转移患者)中的疗效。
• 研究条件:29个国家的98个中心参加的ALEX研究(NCT02075840)。
• 研究时间:2014-08-08至2017-02-09。
• 研究方法:国际多中心、开放性、Ⅲ 期、随机对照临床试验。
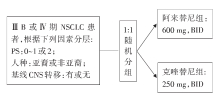
• 研究对象:初治ALK阳性(VENTANA法, D5F3抗体)的Ⅲ B~Ⅳ 期NSCLC患者。无症状脑转移或脑膜转移患者, CNS转移经过放疗后至少14天的患者均可入组。
• 干预措施:患者按1:1比例随机分组, 具体流程见图1。无症状、孤立CNS进展的患者可以根据研究者的判断, 接受局部治疗, 然后继续阿来替尼治疗, 直到全面进展或CNS进展。
• 评价指标:主要研究终点指标为研究者评估的中位无进展生存期(progression-free survival, PFS)。次要研究终点指标包括:独立评审委员会评估的PFS、至CNS进展时间、客观缓解率(objective response rate, ORR)、缓解持续时间、总生存期(overall survival, OS)和安全性。
该研究共入组303例晚期ALK阳性NSCLC患者(阿来替尼组152例, 克唑替尼组151例); 研究的主要终点指标, 即由研究者评估的中位PFS, 阿来替尼组尚未达到[95%可信区间(confidence interval, CI): 17.7个月~未达到], 而克唑替尼组为11.1个月(95%CI 9.1~13.1个月), 风险比(hazard ratio, HR)=0.47, 95%CI 0.34~0.65, P< 0.000 1, 阿来替尼可降低53%疾病进展或死亡风险。
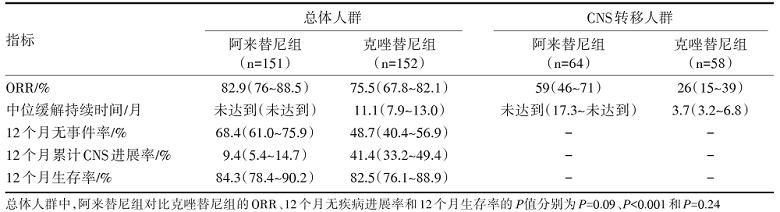
无论是否存在基线CNS转移, 阿来替尼组的12个月累计CNS进展率仅为9.4%(95%CI 5.4%~14.7%), 远低于克唑替尼组的41.4%(95%CI 33.2%~49.4%), 可将CNS疾病进展的风险降低84%(HR=0.16, 95%CI 0.10~0.28, P< 0.000 1); 两组的中位OS均不可估计。见表1。
| 表1 意向性治疗人群的研究者疗效评价结果 |
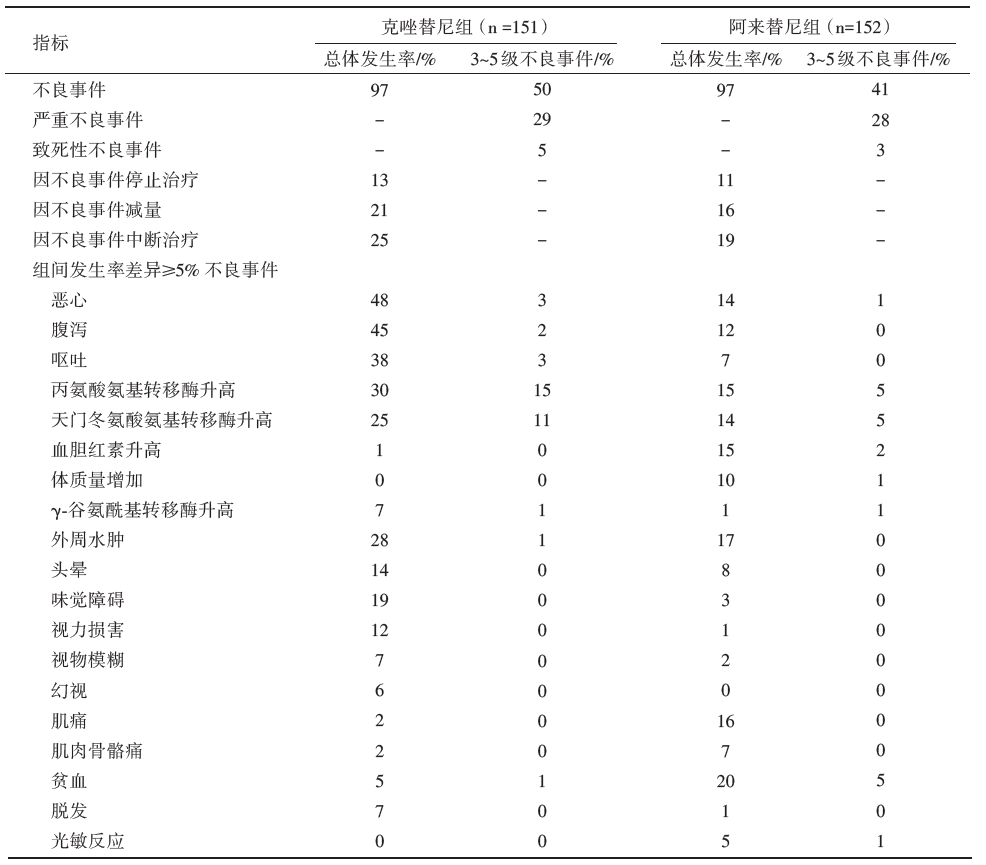
与克唑替尼相比, 阿来替尼对晚期ALK阳性NSCLC的一线治疗显示出更好的全身和CNS疗效、较低的药物毒性。
从2007年, 日本学者首次在NSCLC中发现ALK是非常重要的治疗靶点, 到2011年, 仅4年时间, 克唑替尼就作为第一个ALK抑制剂批准用于治疗ALK阳性晚期NSCLC[1], 开创了肺癌精准医学研究的典范。
ALEX研究是一项国际、多中心的随机Ⅲ 期临床研究, 对比了阿来替尼和克唑替尼一线治疗ALK阳性、合并或不合并无症状CNS转移的晚期NSCLC患者的疗效。患者按1:1比例随机分配接受阿来替尼 600 mg BID(n=152)或克唑替尼 250 mg BID(n=151)治疗。主要终点指标为研究者评估的PFS, 次要终点指标包括:独立评审委员会评估的PFS、至CNS进展时间、ORR和OS。按照预先的统计学假设, 阿来替尼一线治疗ALK阳性NSCLC将中位PFS从克唑替尼组的10.9个月提高到16.8个月, 共需要有170个事件发生, HR=0.65。
2017年ASCO大会上公布了ALEX研究的主要研究终点数据, 并全文发表于《N Engl J Med》[2]。研究共纳入了303例患者, 截止到2017年2月8日, 阿来替尼组68例(45%)患者停止治疗, 而克唑替尼组停止治疗的患者为105例(70%)。164例患者出现疾病进展或死亡, 阿来替尼组为41%(62/152), 克唑替尼组为68%(102/151)。
研究结果显示, 一线接受阿来替尼治疗患者的PFS明显长于克唑替尼, 12个月的无事件生存率为68.4% vs. 48.7%(HR=0.47, P< 0.001)。研究的主要终点指标, 即由研究者评估的中位PFS在克唑替尼组为11.1个月(95%CI 9.1 ~13.1个月), 阿来替尼组还未达到(95%CI 17.7个月~未达到)。研究的次要终点指标之一, 由独立评审委员会评估的中位PFS, 阿来替尼组为25.7个月(95%CI 19.9个月~未达到), 而对照组为10.4个月(95%CI 7.7~14.6个月), HR=0.50, 95%CI 0.36~0.70, P< 0.000 1。同时, 研究数据还表明:阿来替尼可将CNS疾病进展的风险降低84%(HR=0.16, 95%CI 0.10~0.28, P< 0.000 1)。无论是否存在基线CNS转移, 阿来替尼治疗组的12个月累计CNS进展率仅为9.4%(95%CI 5.4%~14.7%), 而克唑替尼组为41.4%(95%CI 33.2%~49.4%)。
2018年的ASCO大会, 更新了ALEX研究继续随访10个月的结果, 一线阿来替尼治疗组的中位PFS达到了34.8个月, 而克唑替尼治疗组的中位PFS为10.9个月(HR=0.43, 95%CI 0.32~0.58), 即相比一代ALK抑制剂, 阿来替尼治疗组的中位PFS延长超过3倍[3]。此外, 无论患者基线是否合并脑转移, 两个治疗组之间都观察到显著的差异。尽管阿来替尼治疗组患者的用药时间更长(27.0个月 vs. 10.8个月), 但3~5级不良事件发生率低于克唑替尼组(44.7% vs. 51.0%)。
ALEX研究是首个头对头对比阿来替尼与克唑替尼一线治疗ALK阳性晚期NSCLC的全球Ⅲ 期临床研究。从研究设计上看, 1:1比例的随机分组保证了统计学效力的最大化, 研究纳入约40%无症状脑转移患者和7%的PS评分为2分的患者, 考虑到了临床实践中患者的真实条件。
ALEX研究中纳入了约45%的亚裔患者, 亚组分析显示亚裔患者从阿来替尼治疗中获益与非亚裔患者一致。在日本进行的J-ALEX研究中, 阿来替尼一线治疗的无进展或死亡风险比为0.34(99.7%CI 0.17~0.71, P< 0.001)[4]。在亚洲进行的ALESIA研究, 也同样验证了阿来替尼对于亚洲人群的疗效和安全性[5]。
阿来替尼是第二代ALK抑制剂, 在药物结构设计中, 通过重塑3D结构进一步优化ALK激酶结构域的结合性、增加了靶向激酶的选择性、改善药物代谢动力学[6]; 与克唑替尼不同, 阿来替尼更容易渗透到CNS中[7], 它不是p-糖蛋白的底物, 不容易被从脑脊液中泵出。所以, 阿来替尼相比其它一代的ALK抑制剂, 有更高的ALK通路选择性及CNS转移的控制作用[8]。
2018年8月, 中国已经批准阿来替尼用于一线治疗ALK阳性晚期NSCLC。不管NCCN指南还是中国的CSCO指南, 也基于阿来替尼的疗效和安全性做出了一线的优先推荐。
ALEX研究更新结果提示, 不同的ALK变体亚型对阿来替尼治疗的PFS未产生影响[3], 但是没有报道不同变体亚型治疗后的耐药机制。从最新在《J Clin Oncol》发表的研究来看[9], ALK不同变体亚型可能会影响到患者的获得性耐药突变。因此, 明确ALK变体亚型, 可以更早地预测患者可能的耐药机制, 从而更有针对性地选择能克服该耐药机制的ALK抑制剂。
另外, 该项研究的OS结果仍未成熟, 考虑到ALK抑制剂家族的药物非常丰富, 患者的后续治疗会直接影响到OS的结果, 最终PFS的完胜能否转换成OS获益仍需要进一步的随访。
但是不可否认的是, 34.8个月的一线治疗PFS确实给ALK阳性晚期NSCLC患者带来了极大的生存希望, 良好的安全性为临床合理用药提供了基本条件。而对于ALK变异体、其他罕见ALK融合亚型以及耐药机制进行的探索, 未来能够真正使ALK阳性晚期NSCLC成为慢性病。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|